編者按:2021年4月15日,《中華人民共和國生物安全法》開始施行,這是生物安全領域的一部基礎性、綜合性、系統性、統領性法律,標志著我國生物安全進入依法治理的新階段。這部法律有哪些重要內容?對生物醫藥產業將產生哪些影響?今日分享國浩律師劉杰、程暢對本法的解讀,以饗讀者。
2020年伊始,一場突如其來的新冠疫情,以令人瞠目結舌的速度肆虐全球,其對人類社會所帶來的沉重影響在未來數年間或許也難以消散。以新冠肺炎為代表的新發傳染病,不僅對人類的生命健康和社會發展產生了巨大的影響,也將生物安全問題以一種觸目驚心的方式推入大眾視野,為人類敲響了生物安全的警鐘。
近年來,國內生物產業發展局面日新月異。從地域分布上看,國內新興生物醫藥產業主要集中于北京、長三角和珠三角地區,主要在北京、江蘇、上海、浙江、廣東等五個省份取得較快發展。但無法回避的問題是,新興生物醫藥產業在為人類健康帶來福祉的同時,也對生物安全構成了新的威脅。
一、《生物安全法》的出臺
在2020年之前,雖然在生物安全的不同領域,基本都有相關的法律法規發揮指引作用和監管效能[注1]。但是,出自科技部、衛健委、生態環境部、農業農村部、自然資源部等多個部門以及地方立法機構的多部行政法規、地方立法、技術規范,在事實上形成了生物安全監管領域政出多門、“九龍治水”的局面[注2]。
基于我國生物安全所面臨的新形勢、新問題以及生物安全監管的現有局面,亟待制定一部法律對先前已有的法律法規、政府規章、地方立法作出整合和統籌,也對新形勢下的新問題作出解答和指引。正是在這樣的背景下,生物安全領域的一部基礎性、綜合性、系統性、統領性法律——《中華人民共和國生物安全法》(以下簡稱《生物安全法》)應運而生。
該部法律明確了生物安全的重要地位和原則,明確堅持中國共產黨對國家生物安全工作的領導,在以下方面全鏈條構建了生物安全風險防控的“四梁八柱”[注3]。

二、《生物安全法》下的監管內容
針對《生物安全法》所規制的內容,筆者擬從重大新發傳染病、動植物疫情防控,生物技術研究、開發與應用安全,病原微生物實驗室生物安全,人類遺傳資源與生物資源安全,生物恐怖與生物武器威脅防范等《生物安全法》所規制的五個主體部分著手,對《生物安全法》所搭建的生物安全風險防控體系進行解讀和論述。
(一) 重大新發傳染病、動植物疫情防控
新冠肺炎疫情自2019年底開始向全球蔓延,迄今為止,已在世界范圍內造成深刻影響,使得多國人民的生活偏離了正常軌道。埃博拉病毒自1976年在剛果(金)的埃博拉河畔首次出現,而后40余年間在非洲爆發10余次,給當地人民以及世界其他國家和地區帶來了嚴重恐慌。在當今時代,隨著人口擴張,人類活動對大自然的不斷侵入,大量人畜共患病不斷出現,給人類社會敲響了疫病防控的警鐘。
在此次《生物安全法》出臺之前,國內關于傳染病防控的有關規定散見于眾多部門法和行政法規中,雖然內容堪稱詳盡,但終究令出多門、權屬不一。
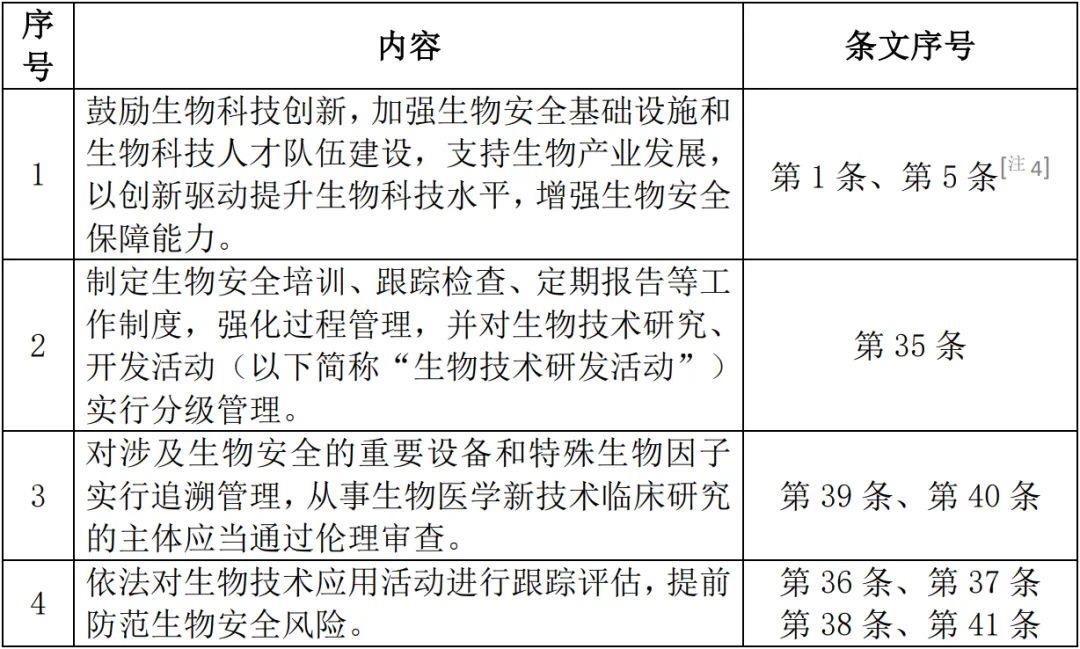
正是在此種局面下,《生物安全法》的出臺,著力優化國內疫病防控領域的監管制度(詳見表1)。
表1:《生物安全法》第三章關于傳染病防控的規定內容

從前述列舉的法規內容可以看出,在該部《生物安全法》的“防控重大新發突發傳染病、動植物疫情”一章中,在確保國務院衛生健康、農業農村、林業草原、海關、生態環境等有關主管部門權屬不變更的情況下,著力搭建一個跨部門的疫情監測、防控體系,既對檢測、報告、預警、防控等流程進行規制,也從進出口防控、與野生動物防疫、抗微生物藥物使用等源頭層面作出了提示。當然,該一傳染病防控體系效用的發揮,顯然離不開《生物安全法》體系下其他監管事項的推進,唯有各方合力,方可發揮最大效用。
(二) 生物技術研究、開發與應用安全
在生物技術高速發展、日新月異的當下,生物技術在給人類疑難雜癥治療提供便利的同時,也留存有對生物安全的威脅。在此次出臺的《生物安全法》中,特設專章以對生物技術研究、開發與應用安全問題作出規制,同時也明確規定了違規從事相關活動的法律責任(詳見表2、表3)。
表2:《生物安全法》關于生物技術研究、開發與應用安全的規定內容
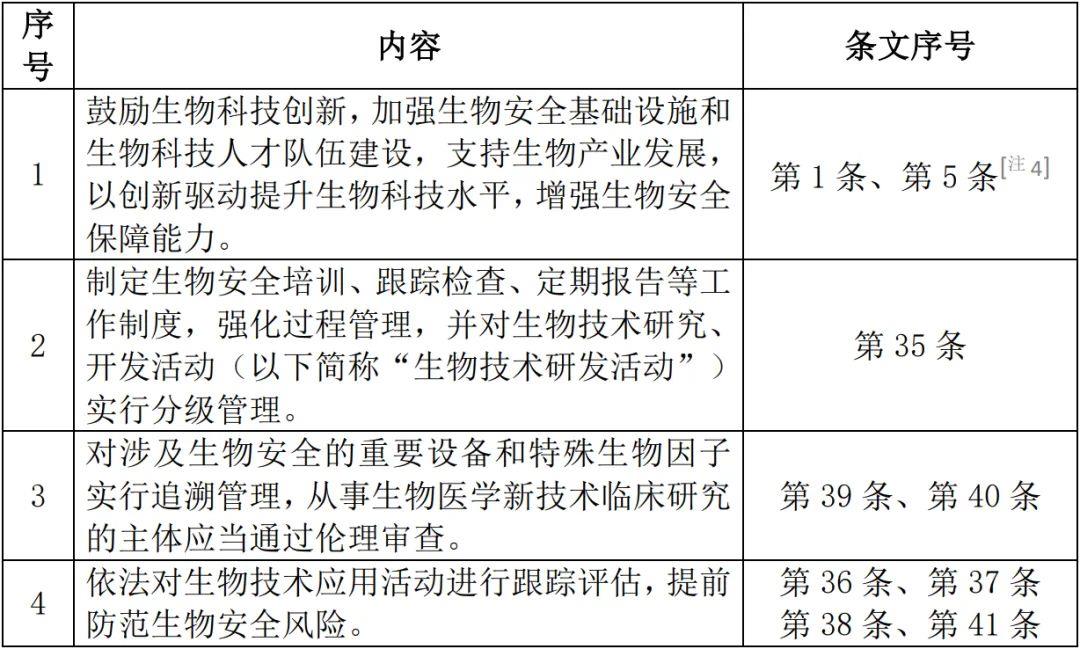
表3:違規從事生物技術研究、開發與應用活動的行政處罰
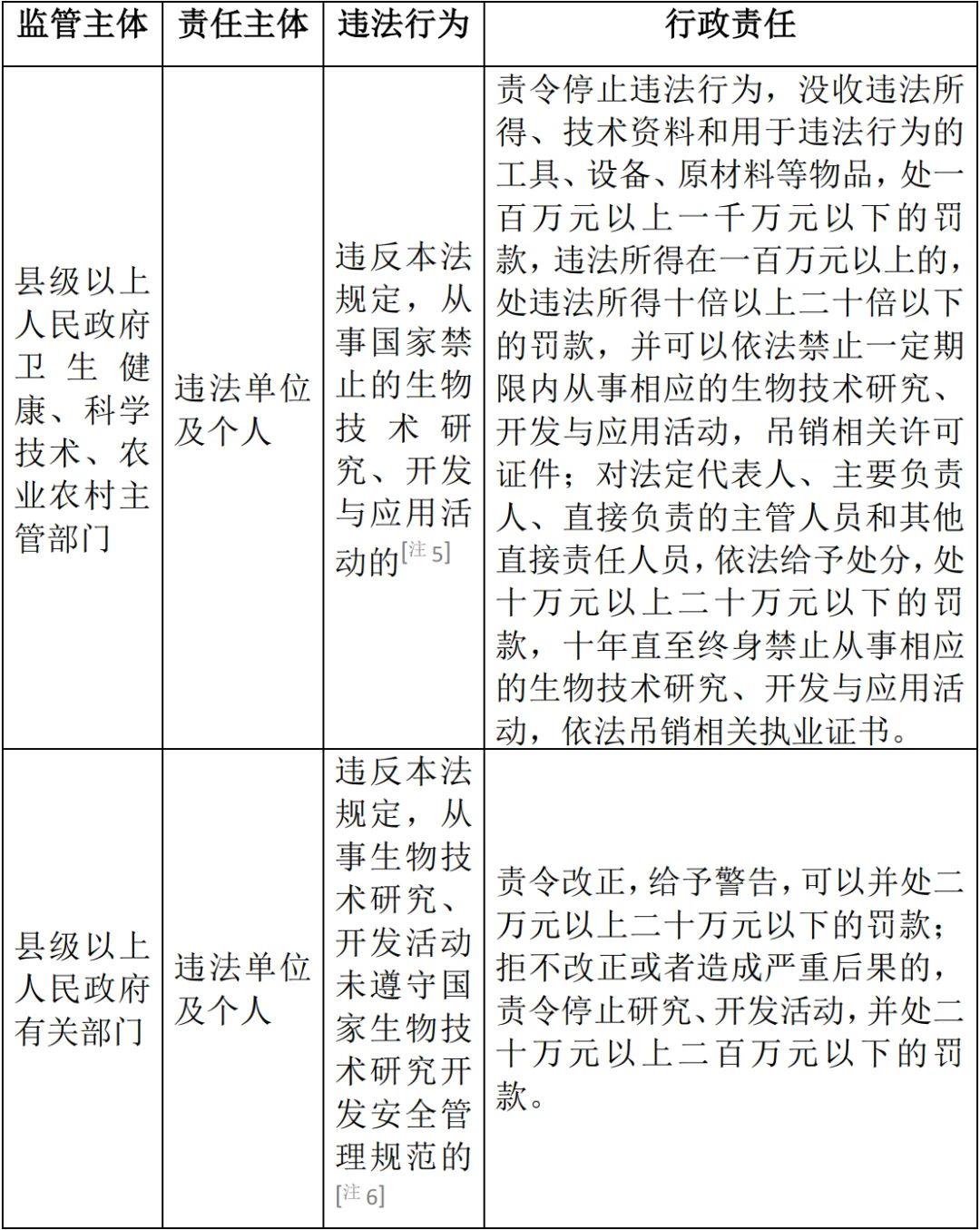
如前文所述,此次出臺的《生物安全法》是生物安全風險監管領域具有提綱挈領、統領全局作用的法律。在生物技術研究、開發及應用方面,根據對公眾健康、工業農業、生態環境等造成危害的風險程度,《生物安全法》將生物技術研發活動分為高風險、中風險、低風險三類[注7]。在開展高風險、中風險生物技術研發活動時,《生物安全法》對研發主體、程序以及風險防控提出了更為嚴格的要求[注8]。但是,除了“對公眾健康、工業農業、生態環境等造成危害的風險程度”這一較為籠統的原則性標準之外,對于一項生物技術研發活動究竟屬于高風險、中風險還是低風險,《生物安全法》并未給出進一步更明確的界限。
在此次《生物安全法》出臺之前,對生物技術研究開發活動進行規制的,是由科學技術部于2017年出臺的部門規范性文件《生物技術研究開發安全管理辦法》(以下簡稱《生物研發管理辦法》)。該《生物研發管理辦法》將生物技術研發活動劃分為三個風險等級:高風險、較高風險和一般風險(詳見表4)。
表4:2017年《生物研發管理辦法》中的風險等級劃分
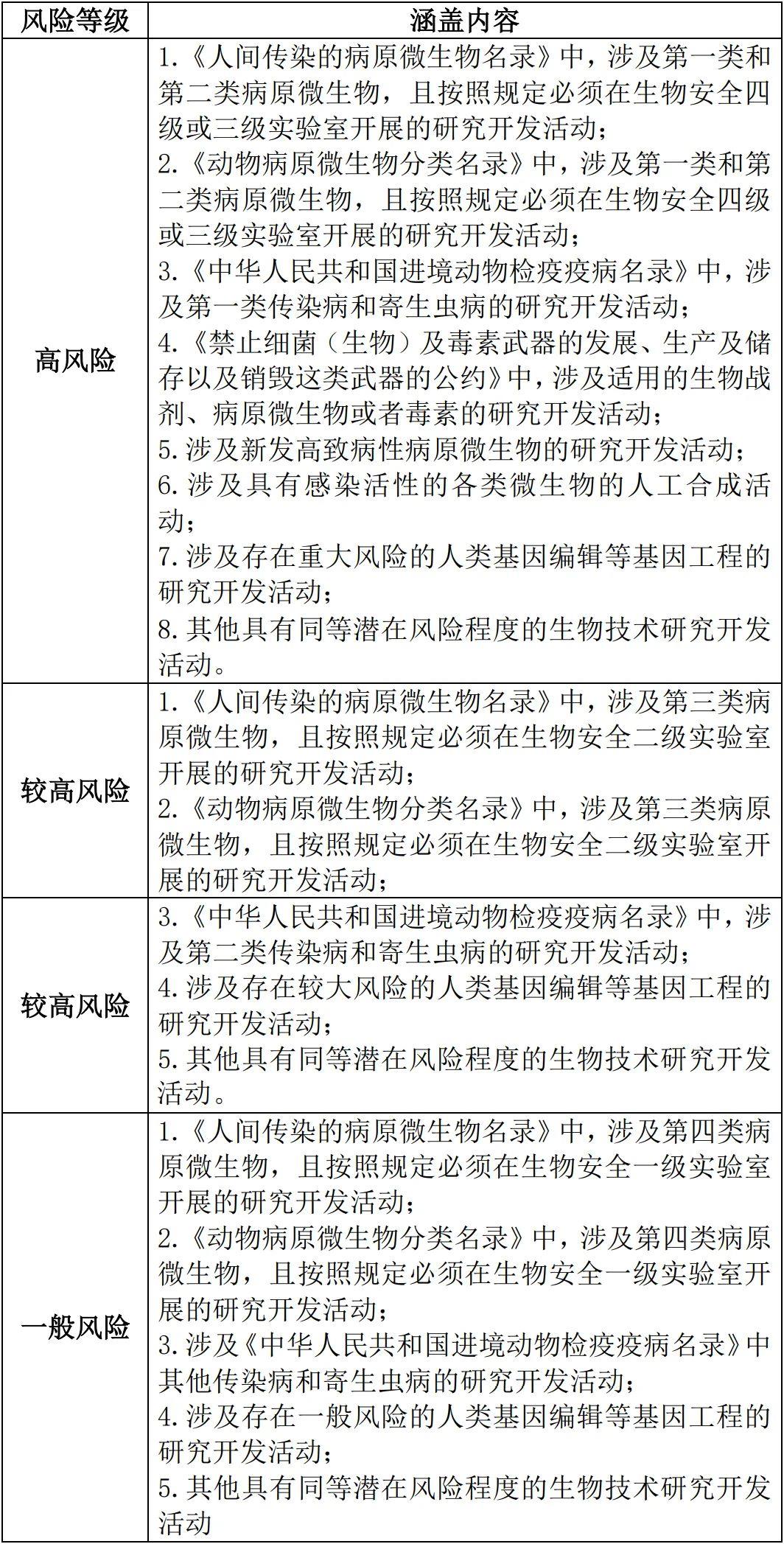
從上表的內容可以看出,2017年《生物研發管理辦法》是以生物技術研發活動所涉物項的風險程度為依據,對生物技術研發活動的風險等級作出劃分。在科學技術部于2019年發布的《生物技術研究開發安全管理條例(征求意見稿)》(以下簡稱《征求意見稿》)中,生物技術研發活動的風險等級被變更為:高風險、一般風險和低風險等3個等級[注9]。同時,風險等級劃分標準也變更為“生物技術研究開發活動及其產品和服務對人類健康、工農業及生態環境等會造成何種負面影響” [注10]。顯然,《生物安全法》中生物技術研發活動風險等級的劃分雖然在具體名稱上與《征求意見稿》有所出入,但是在實質內容上較為接近。在《生物安全法》對生物技術研發活動作出了原則性規定之后,實施細則[注11]仍需要等新的指引文件出臺之后才會有所明確。
(三) 病原微生物實驗室生物安全管理
在新冠肺炎疫情肆虐的背景下,2020年2月15日,科學技術部出臺了《關于加強新冠病毒高等級病毒微生物實驗室生物安全管理的指導意見》,強調各主管部門要加強對實驗室的管理,確保生物安全。這既是當前形勢下規范實驗室生物安全的現實需要,也折射出疫情的爆發使監管機構愈發清醒地認識到對實驗室和科研行為進行監管的極端重要性[注12]。在此次出臺的《生物安全法》第五章中,規定了嚴格的病原微生物實驗室生物安全管理原則,不僅設立病原微生物實驗室需要批準或者備案,而且在分級管理制度下,各等級實驗室的實驗活動權限也受到相應的限制。
對于病原微生物實驗室等級劃分的具體內容,《生物安全法》并未作出規定,僅只提及了低等級、高等級病原微生物實驗室這樣的稱謂[注13]。在科學技術部于2018年修訂完畢的《病原微生物實驗室生物安全管理條例》(以下簡稱《病原微生物實驗室管理條例》)中,明確規定了病原微生物實驗室等級的劃分標準以及各自的權限內容(詳見表5、表6)。
表5:關于病原微生物實驗室等級的劃分
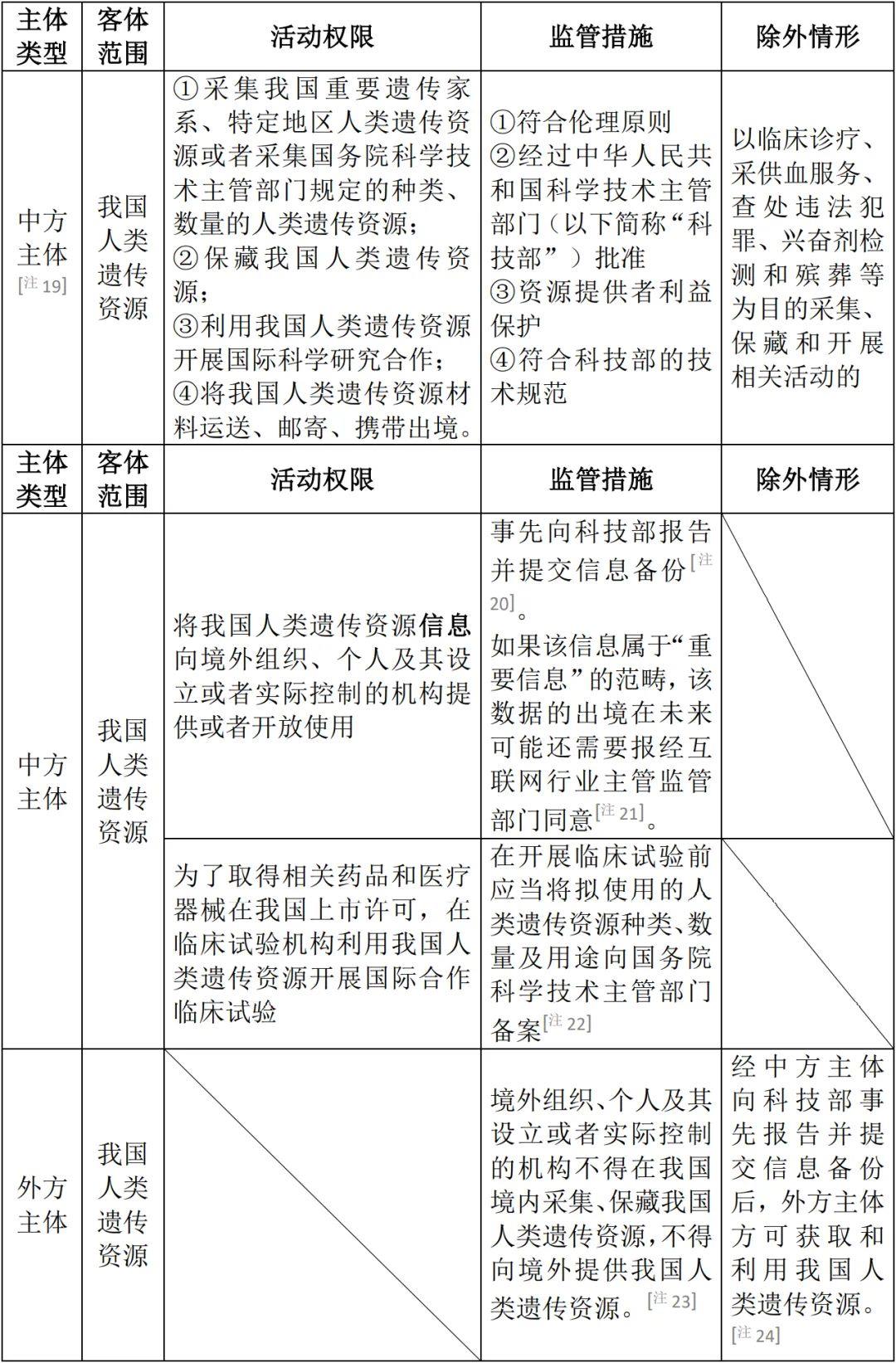
表6:違規病原微生物實驗活動的行政處罰
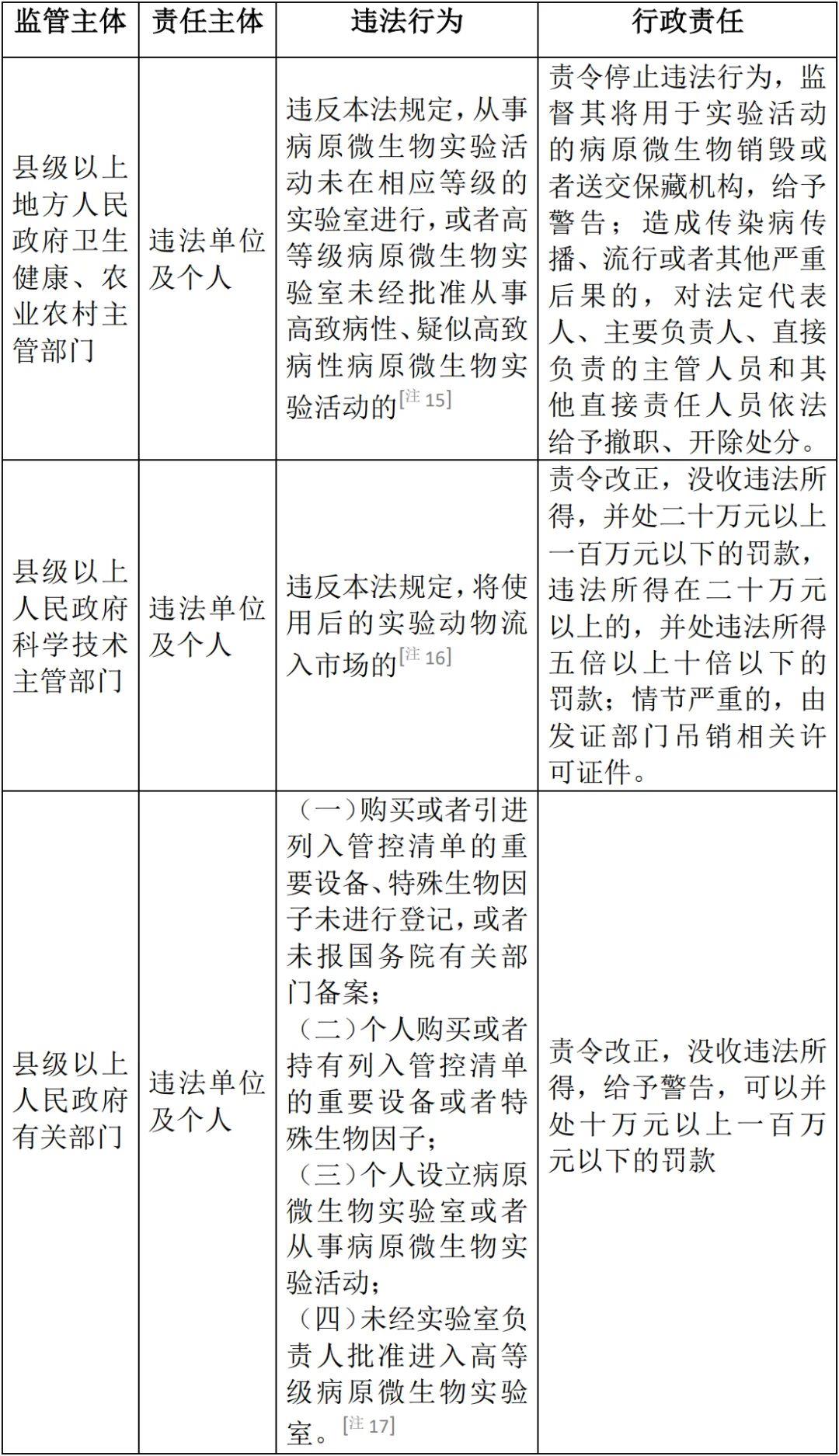
在病原微生物實驗室生物安全監管層面,《生物安全法》在對既有行政法規(如《病原微生物實驗室生物安全管理條例》《實驗動物管理條例》等)進行整合和統籌的基礎上,將相關內容上升到法律的高度并針對違法行為規定了嚴厲的處罰責任,或能促進相關領域的實驗室活動更具規范性和安全性。
(四) 人類遺傳資源與生物資源安全
《生物安全法》第六章規定的是人類遺傳資源與生物資源安全,該部分內容在整部法律中起著承上啟下的作用:一方面,人類遺傳資源與生物資源是生物技術研發活動、病原微生物實驗活動不可或缺的重要材料;另一方面,該兩類資源若被不法利用,則可能嚴重影響一國的生物安全。
1. 人類遺傳資源安全
人類遺傳資源包括人類遺傳資源材料和人類遺傳資源信息。其中,人類遺傳資源材料是指含有人體基因組、基因等遺傳物質的器官、組織、細胞等遺傳材料;人類遺傳資源信息是指利用人類遺傳資源材料產生的數據等信息資料[注18]。
我國對于人類遺傳資源相關的科研和技術活動的監管,始見于1998年的《人類遺傳資源管理暫行辦法》,之后由國務院于2019年出臺了《人類遺傳資源管理條例》(以下簡稱《管理條例》),對采集、保藏、利用、對外提供我國人類遺傳資源的相關活動作出了相應的法律規制,此次出臺的《生物安全法》基本沿襲了《管理條例》的有關規定(詳見表7、表8)。
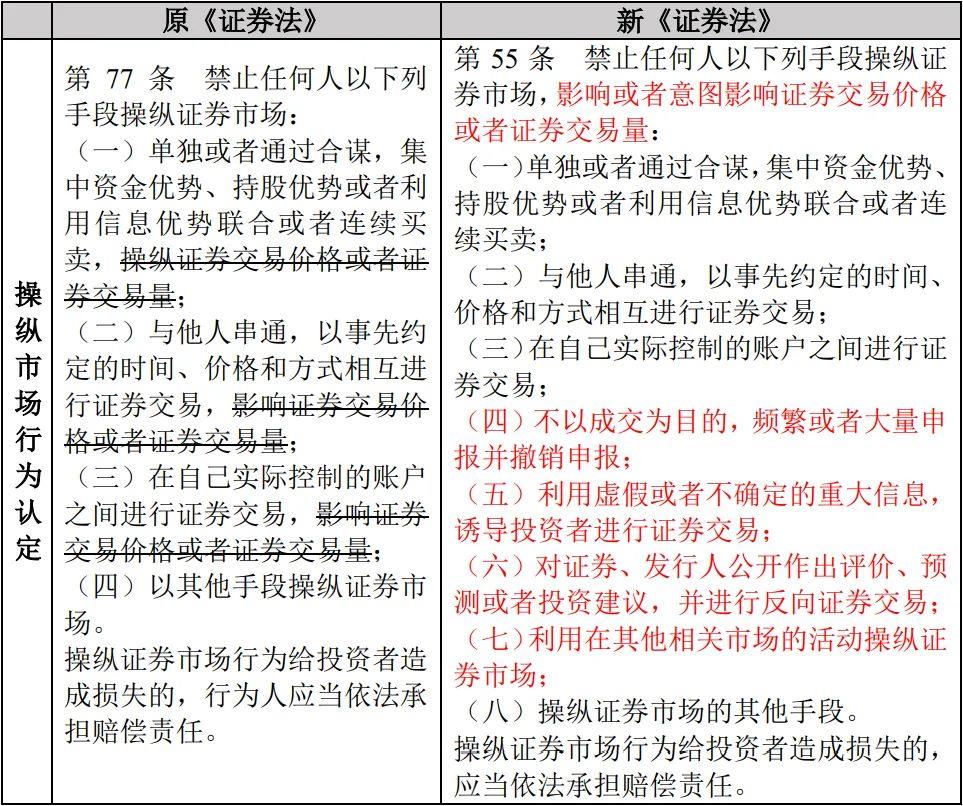
表7:采集、保藏、利用、對外提供人類遺傳資源的規定
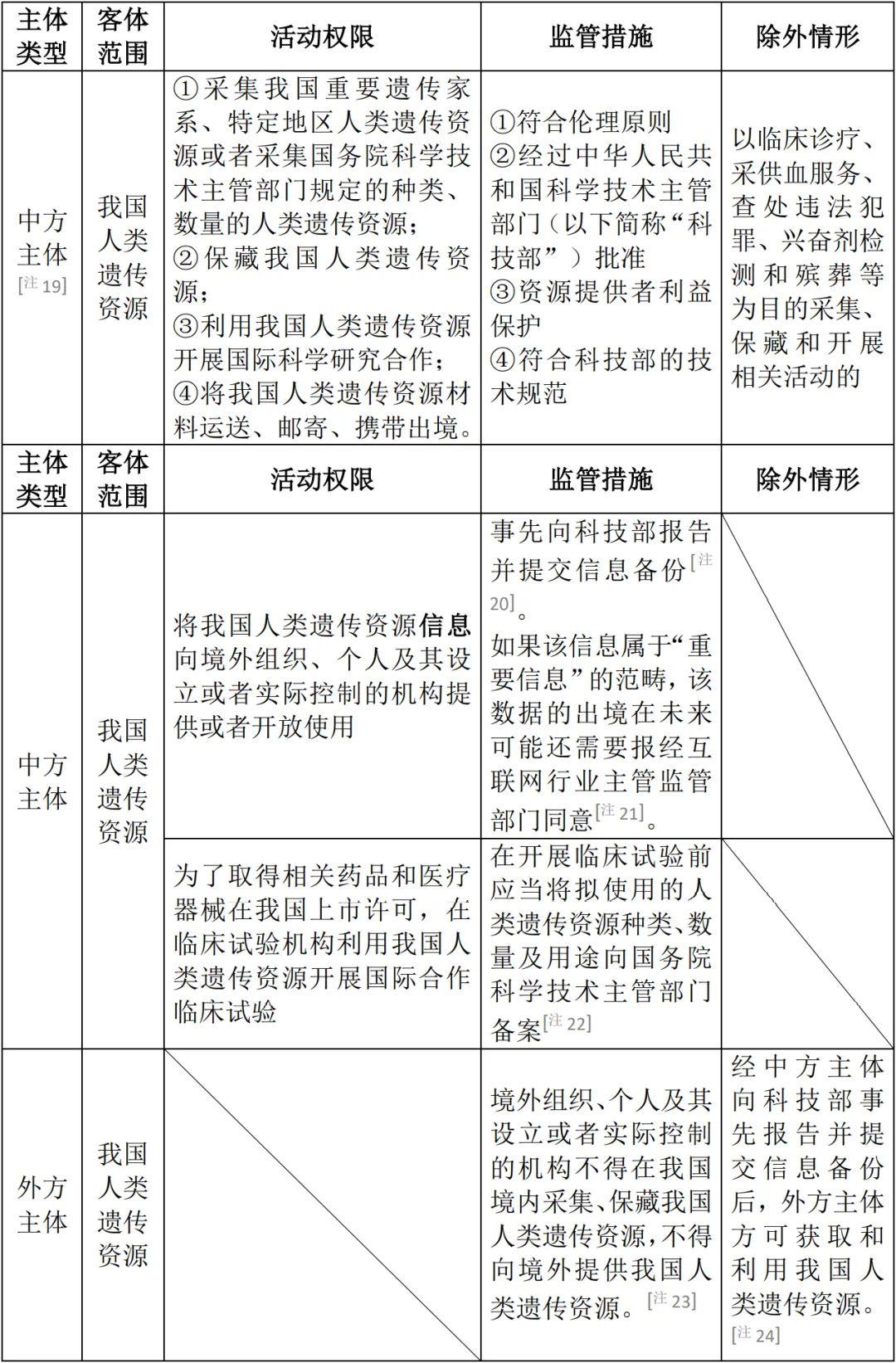
表8:違規參與人類遺傳資源活動的行政處罰
2. 生物資源安全
根據生態環境部于2020年6月22日發布的《2019中國生態環境狀況公報》顯示,全國現已發現660多種外來入侵物種,其中71種對自然生態系統已造成或具有潛在威脅并被列入《中國外來入侵物種名單》[注28]。嚴峻的現實表明,我國生物資源防護工作刻不容緩。雖然早在2015年的《中共中央、國務院關于加快推進生態文明建設的意見》中,就明確指出要“實施生物多樣性保護重大工程,建立監測評估與預警體系,健全國門生物安全查驗機制,有效防范物種資源喪失和外來物種入侵”[注29]。在此次《生物安全法》出臺之前,我國對于生物資源保護和外來物種入侵防范的規定散見于《進出境動植物檢疫法》《動物防疫法》《國境衛生檢疫法》《環境保護法》等部門法和一些地方立法文件中[注30]。
2019年出臺的《生物安全法》不僅從法律上明確了對外來物種入侵的風險防御,保護生物多樣性,維護生態安全的目標價值[注31],同時還提及了相關名錄和清單制度,以及職責劃分和工作開展等事項,有助于全面預防外來物種入侵。
(五) 生物武器與生物恐怖威脅防范
在《生物安全法》第七章,以五個條文對防范生物恐怖與生物武器威脅作出了規定(詳見表9)。
表9:采集、保藏、利用、對外提供人類遺傳資源的規定

從上世紀末到本世紀初,東京地鐵沙林毒氣事件、美國炭疽郵件事件等嚴重生物恐怖襲擊事件,無不使世人談之色變。雖然截止到目前為止,國內并未有遭遇生物恐怖襲擊或生物武器攻擊的案例,但是“安而不忘危,存而不忘亡,治而不忘亂”始終是中國政府防范生物恐怖襲擊的主要思路。此次出臺的《生物安全法》對于該一部分內容的篇幅雖然不多,但是專章設置足以說明對于生物恐怖襲擊和生物武器攻擊的防范,也將會是我國生物安全防控的重點內容。
三、生物醫藥產業風險提示與機遇展望
正如前文所述,《生物安全法》在生物安全防控領域,是一部高屋建瓴的具有基礎性、綜合性、系統性、統領性質的法律,而在具體行為的規制和授權上,現行法規仍駁雜不一。針對這一情況,筆者于此處想要作出進一步的討論,既包括對生物醫藥產業在當前背景下的風險提示,也有此次出臺的《生物安全法》中可能蘊含的機遇。
(一) 產業風險提示
1. 人類遺傳資源相關活動嚴格合規申報
當前新興生物醫藥產業正處于迅猛發展階段,與此同時,外資或者具有外資背景的投資機構在域內生物醫藥產業的布局已成氣候。在實踐中,一個臨床項目的順利開展離不開申報方、醫療機構、臨床CRO、第三方實驗室之間的通力合作,此類產業鏈上的合作伙伴含有外資成分屢見不鮮。故而在實踐中,一個涉及人類遺傳資源的實驗研究活動,受到中國人類遺傳資源管理辦公室的“拷問”幾已成為業內常態。
面對上述情況,對于國內生物醫藥產業而言,一方面,在開展相關實驗或研發活動時需對合作方主體性質審慎判別。另一方面,參照前文列舉的審批和備案要求,相關企業在開展與人類遺傳資源有關的活動時,務必嚴格依照規定履行審批或備案手續,以避免行政處罰風險。
2. 嚴格遵守高致病性病原微生物實驗規范要求
對于生物醫藥產業而言,在進行相關醫藥產品或治療技術的研發過程中,時常會對致病性乃至高致病性病原微生物有所利用。在此種局面下,對于開展類似實驗活動的企業而言,為了確保實驗人員的身體健康及企業的正常運營,都應當對實驗室風險等級規定和實驗室操作規范加以密切關注和嚴格遵守。
除了病原微生物實驗室的安全管理規定之外,對于高致病性病原微生物而言,其運輸、保藏、出口活動都有嚴格的審批或備案要求。因而企業在從事相關活動時,應當嚴格遵守相關規定,筑牢安全防護警戒線。
3. 生物技術研發活動風險等級預案
正如前文所述,當前《生物安全法》對于生物技術研發活動未制定明確的等級劃分標準和相應清單,但是按照2017年《生物研發管理辦法》的相關規定,現有生物企業完全可以對現有研發活動的風險等級作出預估和初步的確定,并做好應對。例如,《生物安全法》規定從事高風險、中風險生物技術研究、開發活動,應當由在我國境內依法成立的法人組織進行,并依法取得批準或者進行備案。
同時,企業應當及時關注主管部門后續出臺的細分性監管文件,包括但不限于科學技術部后續聯合其他部門出臺的風險分類標準和名錄。
4. 謹守倫理審查規范
在《生物安全法》中,“倫理”一詞共出現了4次,雖然次數不多,但是從總則到第四、第六分章均有所體現。在全國人大常委會對《生物安全法(草案)》進行審核前,在立法草案的說明文件中也將生物倫理問題作為重點內容之一,單獨加以說明[注33]。這些都表明生物研發中的倫理問題將得到進一步的探討和重視。
生物醫藥產業的迅速發展,一方面會幫助人類探索出解決各種疑難雜癥的可能性,而在另一方面,以基因技術為代表的生物技術飛速發展也會對既有生物倫理形成挑戰。故而,對相關生物企業而言,除了履行必要的行政程序之外,在研發和應用過程中,還應當重點關注倫理審查和道德倫理要求,謹慎遵守倫理審查規范。
5. 注重數據權利保護
2020年6月28日,《中華人民共和國數據安全法(草案)》(以下簡稱《數據安全法》)經第十三屆全國人大常委會第二十次會議審議,同年7月對外公開征求意見,并將于2021年4月二次審議。這意味著以《中華人民共和國國家安全法》為龍頭的國家安全體系有可能在不久的將來再添一部新法。
在前文探討人類遺傳資源信息時,曾有所提及,一旦人類遺傳資源信息規模足夠龐大,則有可能成為影響國家安全的重要數據[注34]。除此之外,針對大范圍人類遺傳資源信息進行研究所得的結果,一旦泄露也有可能會對國家安全和社會穩定造成影響。在此意義上,數據安全是國家安全密不可分的組成部分,應當予以充分重視。
(二) 展望生物產業機遇
《生物安全法》第一章第一條開宗明義地指出,本法的制定目的之一是為了“促進生物技術健康發展”,第五條表明“國家鼓勵生物科技創新”、“支持生物產業發展”以“增強生物安全保障能力”。這都意味著前沿生物科技研究將受到更多的關注和保障,更有望進一步推動我國在前沿生物科技領域的技術研發創新[注35]。
在生物安全能力建設上我國還有很長的路要走,這其中既有對公民健康教育等軟件設施的進一步普及,也有對高等級生物實驗室、生物技術產品和裝備的龐大需求。如果說前者屬于國家社會保障層面的內容,則后者即有生物產業的機遇存在。能否把握時代機遇,應對國家生物入侵防范、重大疫情防控、生物武器防御、生態環境保護等需求,發展核心競爭力,亟需我國生物產業企業交出自己的答卷。
四、結 語
本文通過對《生物安全法》下重要監管內容的梳理和解讀,嘗試對生物醫藥產業在當前以及今后一個階段所可能面臨的風險和機遇作出提示。如果說突如其來的新冠肺炎疫情,為所有人敲響了生物安全的警鐘。那么這部嶄新出爐的《生物安全法》,即是對國家生物安全提供了強有力的護盾,同時也為國內蓬勃發展的生物醫藥產業厘清了原則和方向。在這樣的局面下,企業應在制度的框架下對照自身情況做好合規工作,以避免監管風險所可能帶來的不必要損失。合規有道,方能行穩致遠。
注釋及參考文獻:
[1] 如在人類遺傳資源管理范疇,有2019年出臺的《中華人民共和國人類遺傳資源管理條例》;在生物兩用物項管理范疇,有2002年出臺的《中華人民共和國生物兩用品及相關設備和技術出口管制條例》;在病原微生物管理范疇,有2018年出臺的《病原微生物實驗室生物安全管理條例》等。
[2] 參見申衛星:《后疫情時代生物安全和中國生物安全的法規對策》,載https://www.sohu.com/a/433563411_120051852,最后訪問時間:2021年3月10日。
[3] 參見《生物安全法表決通過·構建生物安全風險防控“四梁八柱”——全國人大常委會法工委行政法室主任袁杰答記者問》,載http://www.npc.gov.cn/npc/c30834/202010/745f6e57b9b14635a7397be9f92a70e6.shtml,最后訪問時間2021年3月11日。
[4] 本表格中的序號均來自《生物安全法》。
[5] 參見《生物安全法》第74條。
[6] 參見《生物安全法》第75條。
[7] 參見《生物安全法》第36條第1款第2句。
[8] 《生物安全法》第38條規定:“從事高風險、中風險生物技術研究、開發活動,應當由在我國境內依法成立的法人組織進行,并依法取得批準或者進行備案。 從事高風險、中風險生物技術研究、開發活動,應當進行風險評估,制定風險防控計劃和生物安全事件應急預案,降低研究、開發活動實施的風險。”
[9] 參見《生物技術研究開發安全管理條例(征求意見稿)》第10條。
[10] 具體而言,對人類健康、工農業及生態環境等造成嚴重負面影響,威脅國家生物安全,違反倫理道德的潛在風險的研究開發活動,屬于高風險生物技術研究開發活動;具有對人類健康、工農業及生態環境等造成一定負面影響的潛在風險的研究開發活動,屬于一般風險生物技術研究開發活動;對人類健康、工農業及生態環境等不造成或者造成較小負面影響的研究開發活動,低風險生物技術研究開發活動。參見《生物技術研究開發安全管理條例(征求意見稿)》第11條。
[11] 例如《生物安全法》中未明晰的生物技術研發活動風險分類標準及名錄,高風險、中風險生物技術研發活動所涉及的具體審批或備案流程等。
[12] 參見孫佑海:《生物安全法:國家生物安全的根本保障》,載《環境保護》2020年第22期。
[13] 參見《生物安全法》第45條,第46條。
[14] 關于第一類、第二類、第三類、第四類病原微生物的具體劃分,參見《病原微生物實驗室生物安全管理條例》第7條。
[15] 參見《生物安全法》第76條。
[16] 參見《生物安全法》第77條。
[17] 參見《生物安全法》第78條。
[18] 參見《中華人民共和國人類遺傳資源管理條例》第2條。
[19] 根據《管理條例》第21條的規定,“中方單位”指“我國科研機構、高等學校、醫療機構、企業”,“外方單位”指“外國組織及外國組織、個人設立或者實際控制的機構”。具體而言,對于是否屬于中方單位應遵循“穿透三層”(本公司、控股公司以及控股公司的控股公司)的原則,同時公司在國家企業信用信息公示系統上顯示的人員或投資方不能涉及任何外籍人士或外方控股公司。
[20] 參見《生物安全法》第57條。
[21] 國家網信辦于2019年5月發布的《數據安全管理辦法(征求意見稿)》第28條規定:“網絡運營者發布、共享、交易或向境外提供重要數據前,應當評估可能帶來的安全風險,并報經行業主管監管部門同意;行業主管監管部門不明確的,應經省級網信部門批準。 向境外提供個人信息按有關規定執行。”
其第38條第5項規定:“重要數據,是指一旦泄露可能直接影響國家安全、經濟安全、社會穩定、公共健康和安全的數據,如未公開的政府信息,大面積人口、基因健康、地理、礦產資源等。重要數據一般不包括企業生產經營和內部管理信息、個人信息等。”
[22] 參見《生物安全法》第56條第3款。
[23] 參見《生物安全法》第56條第4款。
[24] 參見《生物安全法》第57條,在具體的利用過程中,外方單位需要遵循的監管要求包括:①倫理批準;②一般國際合作項目需要獲得科技部批準;③為獲得相關藥品和醫療器械在我國上市許可,在臨床機構利用我國遺傳資源開展國際合作臨床試驗、不涉及人類遺傳資源材料出境的,在開展臨床試驗前,將擬使用的人類遺傳資源種類、數量及用途向科技部備案;④履行告知義務,征得人類遺傳資源提供者同意;⑤保證中方單位全過程、實質性參與研究;⑥在國際合作活動結束后6個月內與中方單位共同向科技部提交合作研究情況報告。
[25] 參見《生物安全法》第79條。
[26] 參見《生物安全法》第80條。
[27] 參見《生物安全法》第84條。
[28] 參見《2019中國生態環境狀況公報》,第39頁。
[29] 參見《中共中央、國務院關于加快推進生態文明建設的意見》。
[30] 例如《廈門市環境保護條例》《陜西省秦嶺生態環境保護條例》《湖南省外來物種管理條例》等。
[31] 參見《生物安全法》第60條第1款第1句。
[32] 本表格中的序號均來自《生物安全法》。
[33] 參見全國人大環境與資源保護委員會主任委員高虎城:《關于<中華人民共和國生物安全法(草案)>的說明》。
[34] 參見《數據安全管理辦法(征求意見稿)》第38條第5項。
[35] 參見陳娟、李博洋等:《從<生物安全法>出臺看我國生物制造發展機遇》,載《科技中國》2021年第1期。

